العوامل المؤثرة على تفاعل الحمض مع الصخر :
إن معرفة العوامل المؤثرة على التفاعل بالإضافة إلى معرفة ميزات الصخر الخازن يمكن أن يساهم في اختيار نوع الحمض وكميته لتأمين نجاح عملية التحميض .
والعوامل الأساسية المؤثرة هي :
الضغط - الحرارة - تركيز الحمض - سرعة التدفق - التركيب الكيميائي والفيزيائي للصخر - نواتج التفاعل .
- الضغط :
إن سرعة التفاعل بين الحمض والصخور الكربوناتية تتناقص مع زيادة الضغط ، الشكل ، ويلاحظ هذا التناقص جليا عند نطاقات الضغط المخفض أما عند الضغوط الأعلى من (Psi1000 ) فإن تأثير تغييرات الضغط يمكن أن يهمل حيث تأخذ سرعة التفاعل قيمة ثابتة تقريبا مع زيادة الضغط .
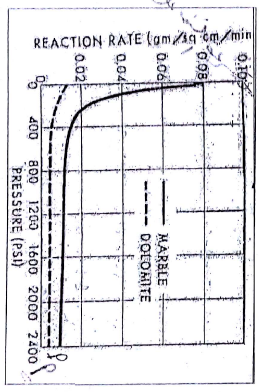
الشكل يوضح علاقة سرعة التفاعل بالضغط للدولومیت والمارل
ويعلل ذلك بوجود Co2 والذي ينحل في الماء الناتج ليغير اتجاه التفاعل التالي :
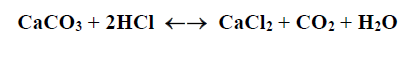
درجة الانحلال هذه تزداد بزيادة الضغط ، ويتجه التفاعل نحو اليسار ويتباطأ أو يتوقف انحلال الكلس ، أما إذا انخفض الضغط فإن CO2 الناتج يكون بشكل غاز ويمكنه الخروج وبالتالي يتجه التفاعل نحو اليمين أي الكلس ينحل بسهولة أكبر أي سرعة التفاعل تزداد .
ويبين الشكل علاقة الضغط مع سرعة التفاعل لحمض كلور الماء مع الحجر الكلسي ومع الدولوميت . ويكون ثاني أوكسيد الكربون بشكل سائل عند الضغط at55 - 70 ولكن بدرجات حرارة أقل من 30°C وهذا ما لا يمكن مصادفته مع الطبقات النفطية وفي كل الأحوال تزداد انحلالية CO2 في السائل الحمضي بزيادة الضغط وبالتالي فإن سرعة التفاعل تتناقص مع تزايد الضغط .
- الحرارة :
إن سرعة تفاعل الحموض تزداد بشكل مباشر بازدياد درجة الحرارة فمعدل تفاعل يتم في درجات حرارة تتراوح بين 140-160 فهرنهايت أكبر بمرتين من معدل تفاعل يتم في درجات حرارة بين 70- 80°f . ونذكر هنا أن درجة الحرارة الفعلية التي تتحكم بتفاعل الحمض يجب أن تأخذ بعين الاعتبار درجة حرارة الحمض المحقون ، ودرجة حرارة الصخر الخازن ، بالإضافة إلى درجة الحرارة المتحررة والناتجة عن التفاعل . ويمكن تلافي تأثير الحرارة التي تزيد من سرعة التفاعل باستخدام مبطئات التفاعل أو عن طريق تبريد شديد للمنطقة القاعية باستخدام الأزوت السائل ، وبذلك يمكن حقن الحمض إلى مسافات أبعد في الطبقة . إن تحميض صخر كلسي بدرجة حرارة °C158 ب HCl تركيزه 10 % يستهلك الحمض خلال 3 دقائق فإذا حقن الحمض بمعدل 1.7 م/ دقيقة فإنه يمكن حقن 5.7 m³ من الحمض فقط قبل تعادله في جبهة الحقن ومن أجل زيادة حجم الحمض المحقون تستخدم مبطئات التفاعل أو تستعمل معدلات ضخ أكبر .
- تركيز الحمض :
عند استعمال سائل حمضي بتركيز قليل يجب ضخ كميات كبيرة من هذا السائل في الطبقة حيث يدخل إلى أعماق كبيرة يصعب عندها إعادة سحبه عند انتهاء عملية المعالجة . أما عند استعمال سائل حمضي بتركيز كبير وبعد انتهاء التفاعل تزداد كثيرة لزوجة السائل بسبب انحلال نواتج التفاعل ( كلور المغنيزيوم - كلور الكالسيوم ) هذه النواتج التي تؤثر على معدل التفاعل الذي ينقص بسببها وبسبب تناقص قوة الحمض ، هذا بالإضافة إلى أن التركيز المرتفع ينشط عمليات تأكل المعدات المستخدمة .
ويبين الشكل العلاقة بين تركيز حمض كلور الماء المتفاعل مع الصخور الكربوناتية وبين معدل التفاعل حيث نلاحظ أن معدل التفاعل يزداد حتى تركيز15- 20 % الزيادة تصل عند حد أقصى هو 24-25% وفوق هذا التركيز فإن معدل التفاعل يتناقص فعليا .
ولقد تم التوصل نتيجة التجارب المخبرية إلى تعيين أفضل تركيز للسائل الحمضي وهو يتراوح بين ( HCl6 - 13% ) وعادة يستعمل التركيز الأعظمي للصخور ذوات النفوذية الضعيفة والحد الأدنى للطبقات ذوات النفوذية الجيدة .
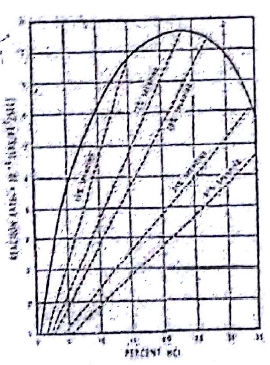
الشكل يبين العلاقة بين تركيز الحمض ومعدل التفاعل
- سرعة التدفق :









